dal-PLAQUE: vasculaire effecten van dalcetrapib onderzocht
04/10/2011
Dalcetrapib moduleert de activiteit van cholesteryl ester transfer protein (CETP) en verhoogt hiermee high-density lipoprotein cholesterol (HDL-C). dal-PLAQUE is de eerste multicenter studie die gebruik maakt van nieuwe niet-invasieve multimodale beeldvorming om structurele en inflammatoire indices van atherosclerose als primaire eindpunten te beoordelen.
De veiligheid en werkzaamheid van dalcetrapib op atherosclerotische aandoeningen met behulp van nieuwe niet-invasieve multimodale beeldvorming (dal-PLAQUE): een gerandomiseerde klinische trialNieuws - 4 okt. 2011
Zahi A Fayad, Venkatesh Mani, Mark Woodward, David Kallend, Markus Abt, Tracy Burgess, Valentin Fuster, Christie M Ballantyne, Evan A Stein, Jean-Claude Tardif, James H F Rudd, Michael E Farkouh, Ahmed Tawakol, for the dal-PLAQUE Investigators
Lancet 2011 DOI:10.1016/S0140-6736(11)61383-4Dalcetrapib moduleert de activiteit van cholesteryl ester transfer protein (CETP) en verhoogt hiermee high-density lipoprotein cholesterol (HDL-C). Na het mislukken van torcetrapib was het onbekend of HDL dat wordt geproduceerd door de interactie met CETP pro-atherogene of pro-inflammatoire eigenschappen had. dal-PLAQUE is de eerste multicenter studie die gebruik maakt van nieuwe niet-invasieve multimodale beeldvorming om structurele en inflammatoire indices van atherosclerose als primaire eindpunten te beoordelen.
Methoden
In deze fase 2b, dubbelblinde, multicenter studie werden patiënten (leeftijd 18-75 jaar) met, of met een hoog risico op coronair hartlijden, gerandomiseerd (1:1) naar dalcetrapib 600 mg/dag of placebo gedurende 24 maanden. Randomisatie werd uitgevoerd met een door de computer gegenereerde randomisatiecode en werd gestratificeerd per centrum. Patiënten en onderzoekers waren gemaskeerd voor de behandeling. Coprimaire eindpunten waren indices die met MRI werden beoordeeld (totale vaatgebied, wandgebied, wanddikte, en genormaliseerde wand index [gemiddelde carotis]) na 24 maanden en beoordeling (met 18F-fluorodeoxyglucose (18F-FDG) PET/CT) van de arteriële ontsteking in een index vat (rechter carotis, linker carotis of stijgende thoracale aorta) na 6 maanden, met no-harm grenzen vastgesteld vóór het opheffen van de blindering van de trial.Analyse was met ‘intention to treat’.
Resultaten
189 patiënten werden gescreend en 130 gerandomiseerd naar placebo (66 patiënten) of dalcetrapib (64 patiënten). Voor de coprimaire MRI en PET/CT-eindpunten waren de confidentie-intervallen onder de no-harm grens of de nadelige verandering was numeriek lager in de dalcetrapib groep dan in de placebogroep. MRI-afgeleide verandering in de totale vat oppervlakte was minder bij patiënten die dalcetrapib kregen in vergelijking met hen die een placebo kregen na 24 maanden; absolute verandering tov baseline vergeleken met placebo was -4.01 mm² (90% CI -7.23 tot -0.80; nominale p = 0.04). De PET/CT meting van de target-to-background ratio (TBR) van het meest aangedane segment van het index vat was niet verschillend tussen de groepen, maar analyse van de halsslagader toonde een verlaging van 7% in de TBR van het meeste aangedane segment in de dalcetrapib groep vergeleken met de placebogroep (-7.3 [90% CI -13.5 tot -0.8]; nominale p = 0.07). Dalcetrapib leidde niet tot een toename van de klinische bloeddruk en de frequentie van bijwerkingen was gelijk tussen de groepen.Interpretatie
Dalcetrapib toonde geen bewijs voor een pathologisch effect op de slagaderwand gedurende 24 maanden. Bovendien suggereert deze studie mogelijk positieve vasculaire effecten van dalcetrapib, waaronder de reductie van de totale vaatvergroting gedurende 24 maanden, maar lange-termijn safety en klinische effectiviteit van dalcetrapib moeten worden geanalyseerd.Achtergrond
De verbetering van de cardiovasculaire uitkomsten bij patiënten met of met een hoog risico op atherosclerotische aandoeningen is nodig, ondanks de aanzienlijke reductie van events bereikt met low-density lipoprotein cholesterol (LDL-C)-verlagende therapieën, in het bijzonder statines.1-3Een mogelijke aanpak om de gevolgen van atherosclerotische plaques te verminderen is het verhogen van high-density lipoprotein cholesterol (HDL-C), 4,5 waarvan epidemiologische studies consistent een omgekeerde relatie hebben aangetoond met het risico van coronaire vaatziekten.6,7 Zelfs in patiënten die met een statine zijn behandeld, zijn lage HDL-C plasmaconcentraties een onafhankelijke risicofactor voor cardiovasculaire gebeurtenissen,8,9 terwijl hogere niveaus van HDL-C zijn geassocieerd met een verminderde plaque progressie10 en een lagere frequentie van cardiovasculaire events.11
Geneesmiddelen die effect hebben op cholesteryl ester transfer protein (CETP) kunnen leiden tot een aanzienlijke toename van het serum HDL-C. Een eerder onderzochte CETP-remmer, torcetrapib, verhoogde het HDL-C effectief, maar werd geassocieerd met een toegenomen mortaliteit,12 waarvan vervolgens gedacht werd dat dat te wijten zou zijn aan stof-specifieke off-target effecten, zoals verhoging van de bloeddruk en vasculaire inflammatie.13 Dalcetrapib is een nieuwe modulator van CETP activiteit die HDL-C doet toenemen.14-16 Tot op heden is de verdraagbaarheid ervan geruststellend, met geen bewijs van klinisch relevante verhogingen van de bloeddruk.15-17 Preklinische experimenten bij konijnen toonden een afname van de atherosclerose met dalcetrapib;18 de directe klinische effecten van dalcetrapib op atherosclerose zijn echter onbekend.
Het primaire doel van de studie was om met een dual-imaging benadering aan te tonen of dalcetrapib een toename van de atherosclerotische plaque progressie of vasculaire ontsteking veroorzaakt in vergelijking met placebo. Deze 24-maanden dal-PLAQUE studie is de langste placebo-gecontroleerde MRI studie met een actief geneesmiddel tot nu toe en eveneens de eerste studie die niet-invasieve multimodale beeldvorming gebruikt voor primaire eindpunten.
Belangrijkste resultaten
Dalcetrapib gegeven gedurende twee jaar deed HDL-C concentraties toenemen met 26.9% (90% CI 20.0 – 33.9%), zonder dat die van low-density lipoprotein cholesterol (LDL-C) en triglyceriden werden beïnvloed.Er werden geen negatieve effecten op de vaatwand of de bloeddruk waargenomen. Dalcetrapib werd geassocieerd met een vermindering van de ontsteking van de carotis vaatwand na 6 maanden (absolute verandering van de gemiddelde carotis target-to-background ratio was -0.19 [90% CI -0.29 - -0.09, p = 0.001] voor dalcetrapib versus -0.04 [-0.14 – 0.06, p = 0.48] voor placebo), alsook een verminderde vaatwand oppervlakte na 24 maanden (absolute verandering ten opzichte van placebo -4.01 mm² [90% CI -7.23 – -0.80, p = 0.04]).
Conclusie
De resultaten van deze klinische studie met niet-invasieve multimodale beeldvorming waarin dalcetrapib werd vergeleken met placebo toonde geen bewijs van een pathologische effect van deze nieuwe CETP modulator.Bovendien leverde MRI het bewijs van een lagere toename van de totale vaatoppervlakte na 24 maanden bij patiënten die dalcetrapib dan bij degenen die placebo kregen. Bovendien leverde PET/CT beeldvorming een observatie van een verband tussen de stijging van de HDL-C concentraties, vermindering van de vasculaire ontsteking, en daaropvolgende vermindering van structurele vasculaire veranderingen. Twee grote lopende klinische studies van dalcetrapib, dal-PLAQUE 2, waarin de progressie van atherosclerotische aandoeningen wordt beoordeeld met coronaire IVUS en carotide B-mode ultrasound (CIMT),19 en dal-OUTCOMES,20 waarin cardiovasculaire morbiditeit en mortaliteit wordt beoordeeld, zullen verder inzicht geven in de therapeutische effecten van dalcetrapib. De imaging methoden die in de dal-PLAQUE werden gebruikt waren om de effecten van dalcetrapib op vasculaire eindpunten te bepalen; voor de bevestiging van de lange-termijn veiligheid en klinische effectiviteit van dalcetrapib wordt de voltooiing van de dal-OUTCOMES afgewacht.
Klik hieronder voor een figuur uit de studie
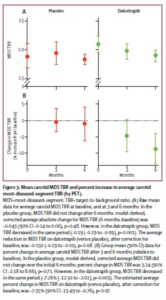
Referenties
1. Scandinavian Simvastatin Survival study group. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival study (4S). Lancet 1994; 344: 1383–89.2. Cannon CP, Braunwald E, McCabe CH, et al. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med 2004; 350: 1495–04.
3. Cholesterol Treatment Trialists’ (CTT) Collaboration, Baigent C, Blackwell L, Emberson J, et al. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170 000 participants in 26 randomised trials. Lancet 2010;376: 1670–81.
4. Chapman MJ, Le Goff W, Guerin M, Kontush A. Cholesteryl ester transfer protein: at the heart of the action of lipid-modulating therapy with statins, fibrates, niacin, and cholesteryl ester transfer protein inhibitors. Eur Heart J 2010; 31: 149–64.
5. Chapman MJ, Ginsberg HN, Amarenco P, et al. Triglyceride-rich lipoproteins and high-density lipoprotein cholesterol in patients at high risk of cardiovascular disease: evidence and guidance for management. Eur Heart J 2011; 32: 1345–61.
6. Gordon T, Castelli WP, Hjortland MC, Kannel WB, Dawber TR. High density lipoprotein as a protective factor against coronary heart disease. The Framingham Study. Am J Med 1977; 62: 707–14.
7. Boden WE. High-density lipoprotein cholesterol as an independent risk factor in cardiovascular disease: assessing the data from Framingham to the Veterans Affairs High-Density Lipoprotein Intervention Trial. Am J Cardiol 2000; 86: 19L–22L.
8. Jafri H, Alsheikh-Ali AA, Karas RH. Meta-analysis: statin therapy does not alter the association between low levels of high-density lipoprotein cholesterol and increased cardiovascular risk. Ann Intern Med 2010; 153: 800–08.
9. Arsenault BJ, Barter P, DeMicco DA, et al. Prediction of cardiovascular events in statin-treated stable coronary patients by lipid and nonlipid biomarkers. J Am Coll Cardiol 2011; 57: 63–69.
10. Johnsen SH, Mathiesen EB, Fosse E, et al. Elevated high-density lipoprotein cholesterol levels are protective against plaque progression: a follow-up study of 1952 persons with carotid atherosclerosis the Tromsø study. Circulation 2005; 112: 498–504.
11. Wei L, Murphy MJ, MacDonald TM. Impact on cardiovascular events of increasing high density lipoprotein cholesterol with and without lipid lowering drugs. Heart 2006; 92: 746–51.
12. Barter PJ, Caulfi eld M, Eriksson M, et al. Effects of torcetrapib in patients at high risk for coronary events. N Engl J Med 2007; 357: 2109–122.
13. Rader DJ. Illuminating HDL—is it still a viable therapeutic target? N Engl J Med 2007; 357: 2180–83.
14. Niesor EJ, Magg C, Ogawa N, et al. Modulating cholesterol ester transfer protein activity maintains efficient pre-β-HDL formation and increases reverse cholesterol transport. J Lipid Res 2010; 51: 3443–54.
15. Stein EA, Stroes ESG, Steiner G, et al. Safety and tolerability of dalcetrapib. Am J Cardiol 2009; 104: 82–91.
16. Stein EA, Roth EM, Rhyne JM, Burgess T, Kallend D, Robinson JG. Safety and tolerability of dalcetrapib (RO4607381/ JTT-705): results from a 48-week trial. Eur Heart J 2010; 31: 480–88.
17. Stroes ESG, Kastelein JJP, Benardeau A, et al. Dalcetrapib: no off -target toxicity on blood pressure or on genes related to the renin-angiotensin-aldosterone system in rats. Br J Pharmacol 2009; 158: 1763–70.
18. Okamoto H, Yonemori F, Wakitani K, Minowa T, Maeda K, Shinkai H. A cholesteryl ester transfer protein inhibitor attenuates atherosclerosis in rabbits. Nature 2000; 406: 203–07.
19. Tardif JC, Lesage F, Harel F, Romeo P, Pressacco J. Imaging biomarkers in atherosclerosis trials. Circ Cardiovasc Imaging 2011; 4: 319–33.
20. Schwartz GG, Olsson AG, Ballantyne CM, et al. Rationale and design of the dal-OUTCOMES trial: effi cacy and safety of dalcetrapib in patients with recent acute coronary syndrome. Am Heart J 2009; 158: 896–901.e3.
