Veelbelovende resultaten met PCSK9 siRNA
Snelle en blijvende daling van PCSK9 en LDL-c niveaus en hoopgevend veiligheidsprofiel in first-in-man fase I studie met siRNA gericht tegen PCSK9
Effect of an RNA interference drug on the synthesis of proprotein convertase subtilisin/kexin type 9 (PCSK9) and the concentration of serum LDL cholesterol in healthy volunteers: a randomised, single-blind, placebo-controlled, phase 1 trialLiteratuur - Fitzgerald et al., Lancet, Okt 2013 - The Lancet, Early Online Publication, 3 October 2013
Fitzgerald K, Frank-Kamenetsky M, Shulga-Morskaya S et al.
The Lancet, Early Online Publication, 3 October 2013 doi:10.1016/S0140-6736(13)61914-5
Achtergrond
Ondanks het veelvuldige gebruik en de effectiviteit van statines, blijft het management van verhoogde LDL-c niveaus ontoereikend, met name in personen met reeds bestaand coronairlijden of diabetes. Het is geschat dat onder hoogrisico-individuen slechts 50% de LDL-c streefwaarden van minder dan 2.59 mmol/L 6 maanden na start van statinebehandeling bereikt, ondanks regelmatige controle en optimalisatie van het behandelregime [1-5]. Dat maakt de noodzaak voor nieuwe behandelingen voor hypercholesterolemie evident.Proprotein convertase subtilisin/kexin type 9 (PCSK9) wordt gezien als een mogelijk therapeutisch doelwit, aangezien experimentele [6-8] en genetische studies [9-11] suggereren dan het verlagen van circulerende plasma PCSK9 niveaus LDL-c niveaus zouden moeten verlagen, en mogelijk ook het risico op coronaire hartziekte. Bovendien lijken statines de circulerende PCSK9 niveaus te verhogen, wat de effectiviteit van statinebehandeling zou kunnen beperken [12-15].
Small interfering RNA (siRNA) kan sequentiespecifieke afbraak van messenger RNA veroorzaken, hetgeen de productie van het bijbehorende eiwit onderdrukt. Dit is onderdeel van het fysiologische RNA interferentie (RNAi) proces [16,17]. Van een PCSK9-specifieke siRNA werd al aangetoond dat het acuut hepatocyte-specifieke productie en plasmaniveaus van PCSK9 verlaagt in preklinische modellen [18], resulterend in een aanzienlijk en voortdurende daling van LDL-c.
Deze gerandomiseerde, enkelvoudig geblindeerde, placebogecontroleerde fase I studie onderzocht de veiligheid en effectiviteit in mensen van intraveneuze toediening van ALN-PCS, een siRNA die PCSK9 productie remt, in een nieuwe lipide-nanopartikelformulering voor toediening [34].
Belangrijkste resultaten
- ALN-PCS was over het algemeen veilig en werd goed getolereerd: er waren geen middelgerelateerde ernstige complicaties. Alle behandelinggeïnduceerde events hadden een milde tot matige ernst, met vergelijkbare proporties van de patiënten in de ALN-PCS- en placebogroep die er last van hadden (19(79%) vs. 7 (88%)).
Zowel patiënten die ALN-PCS als degenen die placebo kregen ontwikkelden een milde maculaire erythemateuze uitslag van voorbijgaande aard, zonder pijn of jeuk. - Er werden geen klinisch significante, dosisafhankelijke veranderingen in labwaarden (inclusief leverfunctietesten, creatine fosfokinase, C-reactive protein, haematologische waarden) opgemerkt, noch in negen gemeten cytokinen.
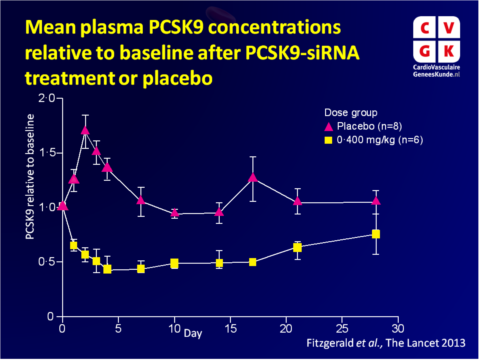
- Eenmalige toediening van ALN-PCS leverde een snelle en dosisafhankelijke afname van PCSK9 plasma-eiwit. De duur van het PCSK9-verlagende effect was dosisafhankelijk.
Bij de hoogste dosering van 0.400 mg/kg, nam PCSK9 af met 70% vanaf baseline, ten opzicht van placebobehandeling, op dag 3 na de dosering (P<0.0001). PCSK9 niveaus stegen significant in de placebogroep, hetgeen werd toegeschreven aan de pre-medicatie die was gegeven aan alle deelnemers. Dit effect werd duidelijk teniet gedaan door ALN-PCS behandeling. - Afname van plasmaniveaus van PCSK9 eiwit was onafhankelijk van baselineniveaus, welke kunnen variëren met een factor 100 binnen een populatie.
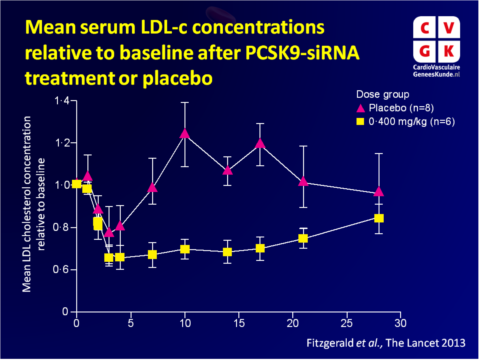
- Een eenmalige dosis ALN-PCS gaf ook een snelle en dosisafhankelijke daling in LDL-c niveaus, weer met een dosisafhankelijke duur. Een gemiddelde reductie van 40% werd bereikt bij de hoogste dosering.
Download Fitzgerald lancet 2013 cvgk.pptx
Conclusie
Deze first-in-man studie laat zien dat ALN-PCS werd goed verdragen; de paar milde tot matige complicaties die in verband werden gebracht met de behandeling, werden zowel in de ALN-PCS als in de placebogroep gezien. Er werden geen andere klinisch relevante veranderingen in leverfunctie of ontstekingsmarkers gezien.Ondanks dat deze studie niet was opgezet met genoeg power om een afname te detecteren, werden significante dalingen van PCSK9 en LDL-c plasmaniveaus gezien bij de hogere dosering. De effecten waren snel en duurden voort.
Referenties
1. Foley KA, Simpson RJ Jr, Crouse JR 3rd, et al. Effectiveness of statin titration on low-density lipoprotein cholesterol goal attainment in patients at high risk of atherogenic events. Am J Cardiol 2003; 92: 79–81.
2. Cholesterol Treatment Trialists’ (CTT) Collaborators. Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90 056 participants in 14 randomised trials of statins. Lancet 2005; 366: 1267–78.
3 Cholesterol Treatment Trialists’ (CTT) Collaborators. Efficacy of cholesterol-lowering therapy in 18 686 people with diabetes in 14 randomised trials of statins: a meta-analysis. Lancet 2008; 371: 117–25.
4 Genest J, McPherson R, Frohlich J, et al. 2009 Canadian Cardiovascular Society/Canadian guidelines for the diagnosis and treatment of dyslipidemia and prevention of cardiovascular disease in the adult—2009 recommendations. Can J Cardiol 2009; 25: 567–79.
4. Foody JM, Sajjan SG, Hu XH, et al. Loss of early gains in low density lipoprotein cholesterol goal attainment among high-risk patients. J Clin Lipidol 2010; 4: 126–32.
5. Horton JD, Cohen JC, Hobbs HH. Molecular biology of PCSK9: its role in LDL metabolism. Trends Biochem Sci 2007; 32: 71–77.
6. Poirier S, Mayer G, Poupon V, et al. Dissection of the endogenous cellular pathways of PCSK9-induced low density lipoprotein receptor degradation: evidence for an intracellular route. J Biol Chem 2009; 284: 28856–64.
7. Rashid S, Curtis DE, Garuti R, et al. Decreased plasma cholesterol and hypersensitivity to statins in mice lacking Pcsk9. Proc Natl Acad Sci USA 2005; 102: 5374–79.
8. Abifadel M, Varret M, Rabes JP, et al. Mutations in PCSK9 cause autosomal dominant hypercholesterolemia. Nat Genet 2003; 34: 154–56.
9. Cohen JC, Boerwinkle E, Mosley TH Jr, Hobbs HH. Sequence variations in PCSK9, low LDL, and protection against coronary heart disease. N Engl J Med 2006; 354: 1264–72.
10. Horton JD, Cohen JC, Hobbs HH. PCSK9: a convertase that coordinates LDL catabolism. J Lipid Res 2009; 50 (suppl): S172–77.
11. Careskey HE, Davis RA, Alborn WEet al. Atorvastatin increases human serum levels of proprotein convertase
subtilisin/kexin type 9. J Lipid Res 2008; 49: 394–98.
12. Davignon J, Dubuc G. Statins and ezetimibe modulate plasma proprotein convertase subtilisin kexin-9 (PCSK9) levels. Trans Am Clin Climatol Assoc 2009; 120: 163–73.
13. Costet P, Hoff mann MM, Cariou B, et al. Plasma PCSK9 is increased by fenofi brate and atorvastatin in a non-additive fashion in diabetic patients. Atherosclerosis 2010; 212: 246–51.
14. Welder G, Zineh I, Pacanowski MA, et al. High-dose atorvastatin causes a rapid sustained increase in human
serum PCSK9 and disrupts its correlation with LDL cholesterol. J Lipid Res 2010; 51: 2714–21.
15. Meister G, Tuschl T. Mechanisms of gene silencing by doublestranded RNA. Nature 2004; 431: 343–49.
16. Vaishnaw AK, Gollob J, Gamba-Vitalo C, et al. A status report on RNAi therapeutics. Silence 2010; 1: 14.
17. Frank-Kamenetsky M, Grefhorst A, Anderson NN, et al. Therapeutic RNAi targeting PCSK9 acutely lowers plasma cholesterol in rodents and LDL cholesterol in nonhuman primates. Proc Natl Acad Sci USA 2008; 105: 11915–20.
18. Jayaraman M, Ansell SM, Mui BL, et al. Maximizing the potency of siRNA lipid nanoparticles for hepatic gene silencing in vivo. Angew Chem Int Ed Engl 2012; 51: 8529–33.
