LDL-hypothese bevestigd met niet-statine therapie, zelfs bij LDL-c niveaus onder streefwaarde
De IMPROVE-IT studie laat zien dat verlagen van LDL-c door toevoeging van de cholesterolabsorptieremmer ezetimibe aan simvastatine CV events verder verlaagt in ACS patiënten met LDL-c volgens aanbevelingen.
Ezetimibe Added to Statin Therapy after Acute Coronary SyndromesLiteratuur - Cannon et al., NEJM 2015
Cannon CP, Blazing MA, Giugliano RP, et al.
NEJM online June 3, 2015. DOI: 10.1056/NEJMoa1410489
Achtergrond
Intensieve statinetherapie verlaagt LDL-c en ook de frequentie van niet-fatale CV events meer dan matige dosering statines, maar residueel risico van CV events blijft bestaan [1-5]. Bovendien is er als gevolg van zorgen omtrent veiligheid in verband met hoge dosering statinebehandeling [6] vraag naar aanvullende lipideverlagende behandeling.Ezetimibe is gericht op het Niemann-Pick C1-like NPC1L1) eiwit, waardoor het absorptie van cholesterol uit de darm remt [7,8]. In aanvulling op statines, verlaagt ezetimibe LDL-c met gemiddeld 23-24% meer [9,10]. Het was totnogtoe onbekend of verdere verlaging van LDL-c niveaus met toevoeging van ezetimibe aan statinebehandeling een klinisch voordeel oplevert.
De Improved Reduction of Outcomes: Vytorin Efficacy International Trial (IMPROVE-IT) evalueerde daarom het effect van ezetimibe gecombineerd met simvastatine (SIM-EZE), ten opzichte van simvastatine monotherapie (SIM), in stabiele patiënten die een acuut coronair syndroom (ACS) hebben doorgemaakt, met LDL-c waarden binnen richtlijn aanbevelingen. 18144 patiënten werden gerandomiseerd naar SIM alleen of SIM-EZE. Na een mediane follow-up van 6 jaar waren 42% van de mensen in beide groepen gestopt met de studiemedicatie, zonder dat zij een primair eindpunt event hadden doorgemaakt of waren overleden.
Belangrijkste resultaten
- Gemiddeld LDL-c niveau ten tijde van ziekenhuisopname voor het index event was 93.8 mg/dL (2.4 mmol/L) in beide groepen. Gedurende de studie was het mediane tijd-gewogen gemiddelde LDL-c 69.5 mg/dL (1.8 mmol/L) in SIM-behandelde patiënten en 53.7 mg/dL (1.4 mmol/L) in patiënten op SIM-EZE (P<0.001).
- In diegenen van wie bloed was afgenomen na 1 jaar, lieten SIM-EZE-behandelde patiënten gemiddeld 16.7 mg/dL (0.43 mmol/L) lagere (P<0.001) LDL-c niveaus zien dan SIM-behandelde patiënten.
- Meer SIM-EZE-behandelde patiënten bereikten het duale doel van LDL-c<70 mg/dL (1.8 mmol/L) en hsCRP < 2.0 na 1 maand (50.6% vs. 30.5% met SIM alleen).
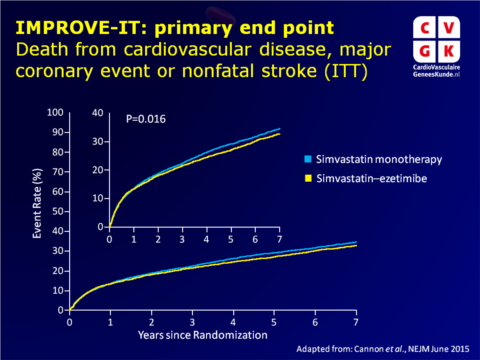
- Een absolute risicoreductie van 2.0 procentpunten voor het primaire eindpunt na 7 jaar werd gezien met toevoeging van ezetimibe (32.7% vs. 34.7%, HR: 0.936, 95%CI: 0.89-0.99, P=0.016), waarvan het voordeel al leek op te treden na 1 jaar.
- De frequentie van dood door CV of willekeurige oorzaken verschilde niet tussen de groepen.
- Risico op enig myocardinfarct (MI) was lager met toevoeging van simvastatine (13.1% vs. 14.8%, HR: 0.87, 95%CI: 0.80-0.95, P=0.002), net als het risico op ischaemische beroerte (3.4% VS. 4.1%, HR: 0.79, 95%CI: 0.67-0.94, P=0.008).
Een niet-significant hoger risico op haemorrhagische stroke werd gezien met toevoeging van EZE (0.8% vs. 0.6%, HR: 0.93-2.04, P=0.11). - Het voordeel van ezetimibe toevoegen aan simvastatine was consistent in bijna alle vooraf gespecificeerde subgroepen, en het leek met name duidelijk in patiënten met diabetes mellitus en in patiënten van 75 jaar of ouder.
- De frequentie van vooraf gespecificeerde veiligheidseindpunten verschilde niet tussen de behandelarmen. 10.1% van de patiënten behandeld met SIM monotherapie en 10.6% op SIM-EZE combinatietherapie staakten behandeling als gevolg van een complicatie.
Conclusie
Toevoeging van het niet-statine middel ezetimibe aan simvastatine verlaagde LDL-c met ongeveer 24% extra en gaf een statistisch significant lager risico op CV events, ten opzichte van simvastatine monotherapie. Er werd geen verschil gezien tussen de behandelgroepen in CV mortaliteit of dood door welke oorzaak dan ook, maar de frequenties van MI en ischaemische beroerte waren significant lager met toevoeging van ezetimibe.Het klinisch voordeel dat werd bereikt met ezetimibe is consistent met dat wat werd gezien met LDL-c verlaging in statinestudies. Hoewel andere lipoproteïnes en hsCRP ook verlaagd waren, ondersteunt de overeenkomst met de observaties in statinestudies de LDL-hypothese die voorspelt dat LDL-c verlaging leidt tot een daling van CV events, zelfs voorbij richtlijn-doelstelling van 70 mg/dL.
Redactioneel commentaar [11]
Ondanks veel bewijs dat de LDL hypothese ondersteunt, waarin LDL-c een causale factor is in het ontstaan van atherosclerotische vasculaire ziekte, blijft discussie bestaan over dat de gunstige effecten van statines niet voldoende verklaard worden door de effecten op LDL-c. Een alternatieve theorie, de ‘statine hypothese’, stelt dat de pleiotrope effecten van statines, die niet gerelateerd zijn aan het lipideverlagende effect, verantwoordenlijk kunnen zijn voor ten minste een deel van het voordeel van statines in het voorkomen van CV events; dus dat statines een unieke effectiviteit hebben in atherosclerotische vaataandoeningen die niet wordt gezien in andere lipideverlagende middelen, en dat het verlagen van LDL-c niet de enige basis voor het gunstige effect van statines is.“IMPROVE-IT is een landmark studie in die zin dat het de eerste klinische studie is die een voordeel laat zien van het toevoegen van een niet-statine lipideverlagend middel aan statinebehandeling.” (…) “ IMPROVE-IT moet niet worden geïnterpreteerd als dat het een uniek voordeel van het gebruik van ezetimibe laat zien. De echte betekenis van IMPROVE-IT is dat het suggereert dat alle dalingen van LDL niveaus, ongeacht het mechanisme, van vergelijkbaar nut zijn. “ (…) “Deze data helpen het primaire nut van LDL-c daling te benadrukken als strategie om coronaire hartziekte te voorkomen. Misschien moet de LDL hypothese nu als het ‘LDL principe’ worden beschouwd.”
Vind dit artikel online bij NEJM
References
1. Cannon CP, Braunwald E, McCabe CH, et al. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med 2004; 350: 1495- 504.
2. de Lemos JA, Blazing MA, Wiviott SD, et al. Early intensive vs a delayed conservative simvastatin strategy in patients with acute coronary syndromes: phase Z of the A to Z trial. JAMA 2004; 292: 1307-16.
3. LaRosa JC, Grundy SM, Waters DD, et al. Intensive lipid lowering with atorvastatin in patients with stable coronary disease. N Engl J Med 2005; 352: 1425-35.
4. Pedersen TR, Faergeman O, Kastelein JJ, et al. High-dose atorvastatin vs usual dose simvastatin for secondary prevention after myocardial infarction: the IDEAL study: a randomized controlled trial. JAMA 2005; 294: 2437-45.
5. Cannon CP, Steinberg BA, Murphy SA, Mega JL, Braunwald E. Meta-analysis of cardiovascular outcomes trials comparing intensive versus moderate statin therapy. J Am Coll Cardiol 2006; 48: 438-45.
6. Preiss D, Seshasai SR, Welsh P, et al. Risk of incident diabetes with intensivedose compared with moderate-dose statin therapy: a meta-analysis. JAMA 2011; 305: 2556-64.
7. Sudhop T, Lutjohann D, Kodal A, et al. Inhibition of intestinal cholesterol absorption by ezetimibe in humans. Circulation 2002; 106: 1943-8.
8. Kosoglou T, Meyer I, Veltri EP, et al. Pharmacodynamic interaction between the new selective cholesterol absorption inhibitor ezetimibe and simvastatin. Br J Clin Pharmacol 2002; 54: 309-19.
9. Ballantyne CM, Blazing MA, King TR, Brady WE, Palmisano J. Efficacy and safety of ezetimibe co-administered with simvastatin compared with atorvastatin in adults with hypercholesterolemia. Am J Cardiol 2004; 93: 1487-94.
10. Morrone D, Weintraub WS, Toth PP, et al. Lipid-altering efficacy of ezetimibe plus statin and statin monotherapy and identification of factors associated with treatment response: a pooled analysis of over 21,000 subjects from 27 clinical trials. Atherosclerosis 2012; 223: 251-61.
11. Jarcho JA, Keany JF. Proof That Lower Is Better — LDL Cholesterol and IMPROVE-IT. NEJM 2015; June 3. DOI: 10.1056/NEJMe1507041
