Twincretine: Superieure glycemische regulatie en gewichtsverlies in vergelijking met GLP-1RA monotherapie in T2DM
In een fase 2b gerandomiseerde trial resulteerde LY3298176, een duale GIP en GLP-1 RA, in statistisch significante en klinisch waardevolle dosis-afhankelijke verbeteringen in glucoseverlaging en gewichtsverlies, in vergelijking met dulaglutide.
Efficacy and safety of LY3298176, a novel dual GIP and GLP-1 receptor agonist, in patients with type 2 diabetes: a randomised, placebo-controlled and active comparator-controlled phase 2 trialLiteratuur - Frias JP, Nauck MA, Van J et al. - The Lancet 2018; published online ahead of print
Introductie en methoden
Glucagon-like peptide-1 receptoragonisten (GLP-RA) zijn geassocieerd met effectieve glycemische regulatie en regulatie van lichaamsgewicht in diabetes type 2 (T2DM), hoewel niet alle patiënten hun doelen behalen met GLP-1 RA therapie [1]. LY3298176 is een synthetisch peptide van 39 aminozuren met agonistactiviteit op zowel glucose-afhankelijke insuline-trofische polypeptide (GIP) en GLP-1 receptoren, dat eenmaal per week onderhuids wordt geïnjecteerd [2]. Deze gerandomiseerde, dubbelblinde, fase 2b studie evalueerde de dosis-respons-relatie van LY3298176 (1, 5, 10, en 15 mg) in T2DM patiënten en onderzocht de effectiviteit en veiligheid in vergelijking met placebo en 1.5 mg dulaglutide.
Voor dit doeleinde werden 316 volwassen patiënten (van 18-75 jaar) met T2DM sinds ten minste 6 maanden en onvoldoende gereguleerd met alleen dieet en lichaamsbeweging of met stabiele metforminetherapie gedurende ten minste 3 maanden voor screening en met een BMI van 23–50 kg/m² (1:1:1:1:1:1) gerandomiseerd naar een van de zes parallelle behandelgroepen gedurende 26 weken (placebo, LY3298176 1, 5, 10, en 15 mg, en de GLP-1 RA dulaglutide 1.5 mg).
De primaire effectiviteitsuitkomst was verandering in HbA1c van baseline tot week 26 in de aangepaste intention-to-treat (mITT) populatie, gedefinieerd als alle deelnemers die ten minste een dosering van de studiemedicatie namen en ten minste een post-baseline meting van elke uitkomst hadden.
Belangrijkste resultaten
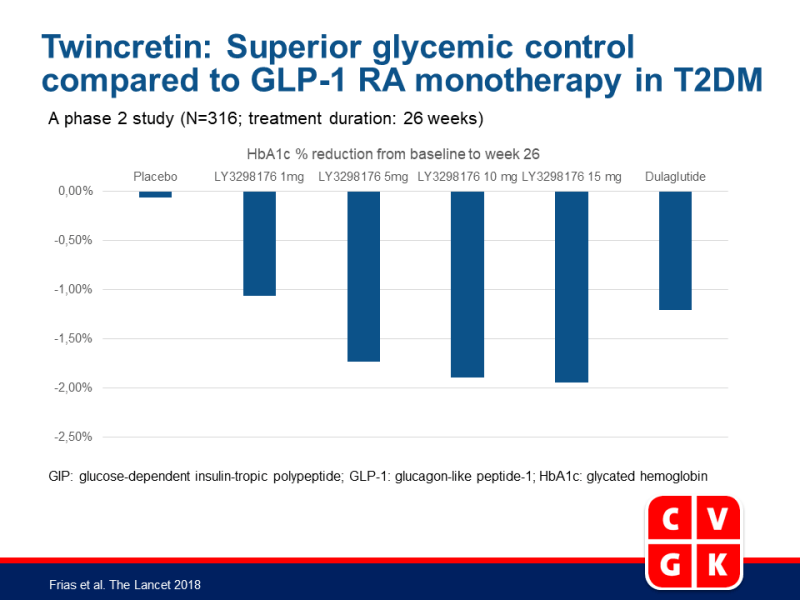
- Gemiddelde veranderingen in HbA1c van baseline tot week 26 met LY3298176 waren –1.06% voor 1 mg, –1.73% voor 5 mg, –1.89% voor 10 mg en –1.94% voor 15 mg, in vergelijking met –0.06% voor placebo en met –1.21% voor dulaglutide.
- Na week 26 behaalde 33–90% van de patiënten behandeld met LY3298176 de HbA1c target van minder dan 7.0% (vs. 52% met dulaglutide en 12% met placebo) en 15–82% behaalde de HbA1c target van ten minste 6.5% (vs. 39% met dulaglutide en 2% met placebo). Deze percentages deelnemers waren het hoogst met 15 mg LY3298176 in vergelijking met dulaglutide (respectievelijk 90.0%, P<0.0001 en 82.0%, P<0.0001).
- Veranderingen in nuchtere plasmaglucose van baseline tot week 26 varieerden van –0.4 mmol/L (–6.8 mg/dL) tot –3.4 mmol/L (–60.7 mg/dL) voor de LY3298176 groepen, in vergelijking met 0.9 mmol/L (15.5 mg/dL) voor placebo en –1.2 mmol/L (–21.2 mg/dL) voor dulaglutide. Grootste verandering in nuchtere plasmaglucose werd gezien met 10 mg LY3298176.
- Veranderingen in gemiddeld lichaamsgewicht van baseline tot week 26 varieerden van –0.9 kg tot –11.3 kg voor de LY3298176 groepen, in vergelijking met –0.4 kg voor placebo en –2.7 kg voor dulaglutide. Alle doses van LY3298176 verlaagden lichaamsgewicht ten opzichte van placebo op een dosis-afhankelijke manier, met een grotere geobserveerde afname in lichaamsgewicht met 5 mg, 10 mg en 15 mg LY3298176, in vergelijking met dulaglutide.
- Na week 26 behaalde 14–71% van diegenen behandeld met LY3298176 de target voor gewichtsverlies van ten minste 5% (vs. 22% met dulaglutide en 0% met placebo) en 6–39% behaalde de target voor gewichtsverlies van ten minste 10% (vs. 9% met dulaglutide en 0% met placebo). Dit percentage deelnemers was het grootst met 15 mg LY3298176 in vergelijking met dulaglutide (respectievelijk 70.6%, P<0.0001 en 39.2%, P<0.0033).
- Veranderingen in gemiddelde tailleomtrek van baseline tot week 26 varieerden van –2.1 cm tot –10.2 cm voor de LY3298176 groepen, met de grootste verandering na behandeling met 15 mg LY3298176, in vergelijking met –1.3 cm voor placebo en –2.5 cm voor dulaglutide.
- Veranderingen in gemiddeld totaal cholesterol van baseline tot week 26 varieerden van 0.2 mmol/L tot –0.3 mmol/L voor LY3298176, in vergelijking met 0.3 mmol/L voor placebo en –0.2 mmol/L voor dulaglutide.
- In de LY3298176 groepen nam het aantal adverse events toe op een dosis-afhankelijke manier, wat voornamelijk werd veroorzaakt door de toegenomen incidentie van milde of matige gastro-intestinale adverse events (LY3298176: 23.1-66.0%, dulaglutide: 42.6% en placebo: 9.8%). Er waren geen meldingen van ernstige hypoglycemie.
Conclusie
In deze fase 2b studie resulteerde LY3298176, een duale GIP- en GLP-1-receptor agonist, in statistisch significante en klinisch waardevolle dosisafhankelijke verbeteringen in glucoseverlaging en gewichtsafname, in vergelijking met dulaglutide en placebo.
Redactioneel commentaar
In hun redactionele commentaar merken Stumvoll en Tschöp [4] op dat het te vroeg is voor een verreikende conclusie op basis van de resultaten verkregen in de studie van Frias et al.. Verschillende vragen blijven nog onbeantwoord, zoals of LY3298176 superieur is aan semaglutide, de meest effectieve GLP-1 RA, welke patiënten het meest baat hebben bij duale agonisten en wat de optimale dosering is. Naarmate het veld zich ontwikkelt in de richting van metabole precisie-geneeskunde, kunnen toekomstige besluitvormingsprocessen bestaan uit het identificeren van de beste incretine-gebaseerde therapie voor elke individuele patiënt, met keuze uit combinaties van single-molecule-geneesmiddelen. Beter begrip van de respectievelijke werkingsmechanismen en betrouwbare voorspellende markers zullen van grote waarde zijn om dergelijke behandelkeuzes op de juiste manier te personaliseren. De auteurs concluderen: ‘De gezamenlijke interpretatie van bemoedigende resultaten van farmacologisch geoptimaliseerd GLP-1 mono-agonisme en deze nieuwe observaties wijzen op superieure voordelen van een aanpak met twincretine, suggereren dat deze behandelbenaderingen zouden kunnen bijdragen aan pogingen om de toenemende prevalentie van obesitas en diabetes type 2 te verlagen’.
Referenties
1. Nauck MA, Meier JJ. The incretin effect in healthy individuals and those with type 2 diabetes: physiology, pathophysiology, and response to therapeutic interventions. Lancet Diabetes Endocrinol 2016; 4: 525–36.
2. Tamer C, Sloop KW, Loghin C, et al. LY3298176, a novel dual GIP and GLP-1 receptor agonist for the treatment of type 2 diabetes mellitus: from discovery to clinical proof of concept. Mol Metab (in press).
3. Stumvoll M and Tschöp M. Twice the benefits with twincretins? The Lancet 2018; published online ahead of print.
