LVEF tijdens ziekenhuisopname voor acuut HF is een onafhankelijke voorspeller van klinische uitkomsten
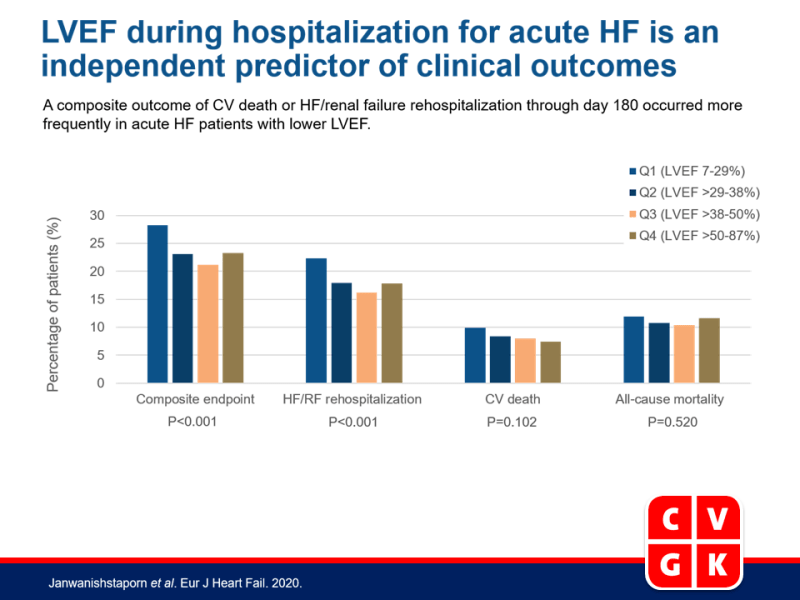
De samengestelde uitkomst van CV sterfte of heropname door HF/nierfalen tot dag 180 kwam vaker voor bij acute HF patiënten met een lagere LVEF.
Relationship between left ventricular ejection fraction and cardiovascular outcomes following hospitalization for heart failure: insights from the RELAX-AHF-2 trialLiteratuur - Janwanishstaporn S, Feng S, Teerlink J. et al., - Eur J Heart Fail. 2020. doi: 10.1002/ejhf.1772.
Introductie en methoden
Ziekenhuisopname voor acute HF (AHF) is een voorspeller voor heropname en CV sterfte in de maanden na ontslag [1]. Dit risico verschilt echter bij HF patiënten vanwege de heterogeniteit van de HF populatie. Informatie over de omvang van het risico bij patiënten met AHF na ziekenhuisopname is van belang om de richting van medische behandeling te bepalen [2-4]. Linkerventrikelejectiefractie (LVEF) is een nuttige maat bij het bevestigen van de diagnose van HF en bij het opstellen van aanbevelingen voor medische therapieën [5]. De waarde van LVEF bij het voorspellen van klinische uitkomsten van patiënten met AHF na ziekenhuisopname is echter nog onduidelijk. Deze studie evalueerde de relatie tussen LVEF gemeten tijdens AHF ziekenhuisopname en de uitkomsten na ontslag in de Relaxin in Acute Heart Failure 2 (RELAX-AHF-2) studie.
De RELAX-AHF-2 was een multicenter, gerandomiseerde, dubbelblinde, placebo-gecontroleerde fase 3-studie die opgenomen patiënten met AHF includeerde [6]. Patiënten werden gerandomiseerd en ontvingen ofwel serelaxine gedurende 48 uur of een gematchte placebo. De twee behandelarmen werden in de huidige analyses samengevoegd vanwege het neutrale effect van serelaxine op de bestudeerde uitkomsten, bestaande uit CV sterfte en verslechterend HF [7]. 6128 Patiënten werden geïncludeerd in de huidige analyses. Patiënten werden geclassificeerd in kwartielen op basis van LVEF gemeten tijdens indexopname in het ziekenhuis: Q1, LVEF 17-29% (n=1548); Q2, LVEF> 29-38% (n=1556); Q3, LVEF> 38-50% (n=1815) en Q4, LVEF> 50-87% (n=1209). LVEF werd ook geanalyseerd als een continue variabele.
De primaire samengestelde uitkomst was CV sterfte of HF/nierfalen (RF) heropname tot dag 180. Andere uitkomsten waren de twee componenten van de samengestelde uitkomst afzonderlijk en sterfte door alle oorzaken tot dag 180.
Belangrijkste resultaten
- Voor het primaire samengestelde eindpunt werden significante verschillen tussen kwartielen gevonden met de hoogste frequentie bij patiënten in kwartiel 1 (28.2% in Q1 versus 23.3% in Q4, P<0.001). Er werden ook significante verschillen tussen kwartielen gevonden voor heropname van HF/RF tot 180 dagen (22.3% in Q1 vs. 17.8% in Q4, P <0.001), maar niet voor CV sterfte of sterfte door alle oorzaken.
- Elke toename van 5% in LVEF was geassocieerd met een significante vermindering van het risico voor het samengestelde eindpunt (gecorrigeerde HR 0.97, 95%CI 0.94-0.99, P= 0,009) en voor HF/RF heropname tot dag 180 (gecorrigeerde HR 0.95, 95%CI 0.93-0.98, P <0.001).
- Een smooth spline curve toonde dat het risico voor het samengestelde eindpunt stabiel bleef als LVEF afnam totdat deze een waarde van ongeveer 40% bereikte. Onder deze LVEF-waarde nam het risico progressief toe. Een vergelijkbaar patroon werd gevonden voor HF/RF heropname. Er werd geen significante associatie gevonden tussen LVEF en sterfte door alle oorzaken.
- Patiënten met een ischemische etiologie hadden een hoger risico op het samengestelde eindpunt dan diegenen met een niet-ischemische etiologie. Er werd een significant verschil waargenomen in de samengestelde uitkomst over LVEF-kwartielen bij patiënten met een ischemische etiologie (P<0.0001 met log-ranktest) (P-interactie=0.019). Dit was minder robuust bij patiënten met een niet-ischemische etiologie (P=0.039). Risico op het samengestelde eindpunt was groter bij patiënten met een lagere LVEF bij wie het indexevent werd veroorzaakt door decompensatie van bestaande HF (P <0.0001 door log-ranktest), maar niet bij patiënten met de novo HF (P-interactie 0.047).
Conclusie
Bij patiënten die met AHF in het ziekenhuis waren opgenomen kwam de samengestelde uitkomst van CV sterfte of HF/RF heropname tot dag 180 significant vaker voor bij patiënten in het laagste LVEF kwartiel, vergeleken met patiënten in het hoogste kwartiel. Dit resultaat werd voornamelijk veroorzaakt door een hoger risico op HF/RF heropname. Het risico op de samengestelde uitkomst en HF/RF heropname nam progressief toe als LVEF daalde onder 40%.
Referenties
1. Go YY, Sellmair R, Allen JC Jr, Sahlen A, Bulluck H, Sim D, Jaufeerally FR, MacDonald MR, Lim ZY, Chai P, Loh SY, Yap J, Lam CS. Defining a ‘frequent admitter’ phenotype among patients with repeat heart failure admissions. Eur J Heart Fail 2019;21:311–318.
2. Miro O, Rossello X, Gil V, Martin-Sanchez FJ, Llorens P, Herrero-Puente P, Jacob J, Bueno H, Pocock SJ. Predicting 30-day mortality for patients with acute heart failure in the emergency department: a cohort study. Ann Intern Med 2017;167:698–705.
3. Peterson PN, Rumsfeld JS, Liang L, Albert NM, Hernandez AF, Peterson ED, Fonarow GC, Masoudi FA. A validated risk score for in-hospital mortality in patients with heart failure from the American Heart Association Get With the Guidelines program. Circ Cardiovasc Qual Outcomes 2010;3:25–32.
4. Lee DS, Lee JS, Schull MJ, Borgundvaag B, Edmonds ML, Ivankovic M, McLeod SL, Dreyer JF, Sabbah S, Levy PD, O’Neill T, Chong A, Stukel TA, Austin PC, Tu JV. Prospective validation of the Emergency Heart Failure Mortality Risk Grade for acute heart failure. Circulation 2019;139:1146–1156.
5. Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JG, Coats AJ, Falk V, González-Juanatey JR, Harjola VP, Jankowska EA, Jessup M, Linde C, Nihoyannopoulos P, Parissis JT, Pieske B, Riley JP, Rosano GM, Ruilope LM, Ruschitzka F, Rutten FH, van der Meer P. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2016;18:891–975.
6. Teerlink JR, Voors AA, Ponikowski P, Pang PS, Greenberg BH, Filippatos G, Felker GM, Davison BA, Cotter G, Gimpelewicz C, Boer-Martins L,Wernsing M, Hua TA, Severin T, Metra M. Serelaxin in addition to standard therapy in acute heart failure: rationale and design of the RELAX-AHF-2 study. Eur J Heart Fail 2017;19:800–809.
7. Metra M, Teerlink JR, Cotter G, Davison BA, Felker GM, Filippatos G, Greenberg BH, Pang PS, Ponikowski P, Voors AA, Adams KF, Anker SD, Arias-Mendoza A, Avendaño P, Bacal F, Böhm M, Bortman G, Cleland JGF, Cohen-Solal A, Crespo-Leiro MG, Dorobantu M, Echeverría LE, Ferrari R, Goland S, Goncalvesová E, Goudev A, Køber L, Lema-Osores J, Levy PD, McDonald K, Manga P, Merkely B, Mueller C, Pieske B, Silva-Cardoso J, Špinar J, Squire I, Stepinska J, Van Mieghem W, von Lewinski D, Wikström G, Yilmaz MB, Hagner N, Holbro T, Hua TA, Sabarwal SV, Severin T, Szecsödy P, Gimpelewicz C; RELAX-AHF-2 Committees and Investigators. Effects of serelaxin in patients with acute heart failure. N Engl J Med 2019;381:716–726.
Download de slideVind dit artikel online op Eur J Heart Fail.
