Type CVD bij baseline beïnvloedt CV voordelen met SGLT2-remming
Een meta-analyse van drie CVOT’s liet alleen matig voordeel zien van SGLT2-remmers op atherosclerotische MACE in diegenen met ASCVD, terwijl dit robuust voordeel gaf op HHF en nierziekte ongeacht CVD of HF bij baseline.
SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trialsLiteratuur - Zelniker TA, Wiviott SD, Raz I et al. - The Lancet 2018: published online ahead of print
Introductie en methoden
Hoewel natrium-glucose cotransporter-2 remmers (SGLT2-i) aanbevolen worden om risico op MACE te verlagen in patiënten met atherosclerotische cardiovasculaire ziekte (ASCVD) maar niet in diegenen met alleen meerdere risicofactoren [1,2], blijft het onbekend of de CV effectiviteit van SGLT2-i afhankelijk is van baseline ASCVD risicocategorieën, een voorgeschiedenis van HF of nierfunctie. De publicatie van de DECLARE-TIMI 58 resultaten [3] maakt nu betere studie mogelijk van de potentiële heterogeniteit in CV effectiviteit op basis van baseline CVD risico. Bovendien maakt een meta-analyse een betere beoordeling mogelijk van enkele zeldzame adverse events die zijn waargenomen in sommige van de CVOT’s met SGLT2-remming.
Daarom combineerde deze meta-analyse data van alle grootschalige placebo-gecontroleerde CVOT’s met SGLT2-i die gepubliceerd zijn tot sept 2018 (EMPA-REG OUTCOME, CANVAS Program en DECLARE-TIMI 58 trials; n=34322) om meer betrouwbare schattingen te verkrijgen van effectiviteit en veiligheid van specifieke uitkomsten in het algemeen en in relevante subgroepen. De DECLARE-TIMI 58 includeerde ook patiënten zonder ASCVD maar met meerdere risicofactoren (59%) en in het gepoolde cohort vertegenwoordigde deze groep 39.8%. Deze subgroepen bestonden uit: ASCVD vs. meerdere risicofactoren, met vs. zonder een voorgeschiedenis van HF en eGFR levels (laag: <60 mL/min/1.73m², middelste: 60-90 mL/min/1.73m² en hoog: ≥90 mL/min/1.73m²).
Effectiviteitsuitkomsten waren MACE, de samenstelling van CV sterfte of ziekenhuisopname voor HF, hun individuele componenten, en een gestandaardiseerde samenstelling van renale uitkomsten waaronder verslechtering van eGFR, eindstadium nierziekte of renale sterfte. Veiligheidsuitkomsten waren niet-traumatische amputaties van de onderste ledematen, fracturen en diabetische ketoacidose.
Belangrijkste resultaten
Effectiviteitsuitkomsten: verschillende subgroepen
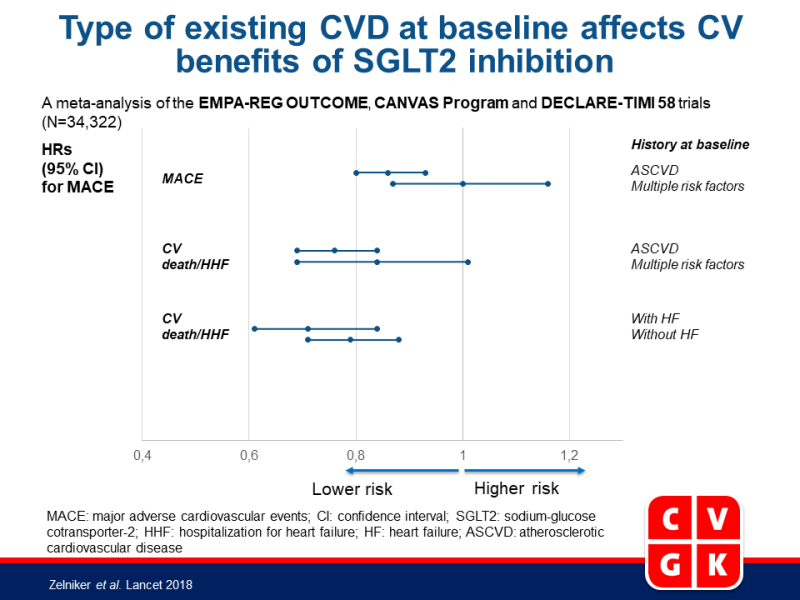
- In totaal verlaagden SGLT2-i het risico op MACE met 11% (HR: 0.89, 95%CI: 0.83-0.96, P=0.0014). Bij stratificatie van geschiedenis met ASCVD, werd dit effect alleen in patiënten met ASCVD gezien (HR: 0.86, 95%CI: 0.80-0.93, P=0.0002), maar niet in patiënten met meerdere risicofactoren (HR: 1.00, 95%CI: 0.87-1.16, P=0.98) (P-interactie=0.0501).
- In patiënten met ASCVD verlaagden SGLT2-remmers het risico op MI (HR: 0.85, 95%CI: 0.76-0.95) en CV sterfte (HR: 0.80, 95%CI: 0.71-0.91), terwijl geen effect werd gezien in patiënten zonder ASCVD. In beide groepen beïnvloedde SGLT2-remming stroke niet significant.
- In totaal verlaagden SGLT2-i significant het risico op de samenstelling van CV sterfte of HHF met 23% (HR: 0.77, 95%CI: 0.71-0.84, P<0.0001). In patiënten met ASCVD was de HR voor de samenstelling van CV sterfte of HHF 0.76 (95%CI: 0.69-0.84, P<0.0001) en in patiënten met meerdere risicofactoren was deze 0.84 (95%CI: 0.69-1.01, P=0.0634) (P-interactie=0.41).
- De reductie in de samenstelling van CV sterfte of HHF was niet significant verschillend in patiënten met (HR: 0.71, 95%CI: 0.61-0.84, P<0.0001) of zonder (HR: 0.79, 95%CI: 0.71-0.88, P<0.0001) een voorgeschiedenis van HF bij baseline (P-interactie=0.51). De uitkomsten van de individuele componenten verschilden evenmin tussen deze groepen.
- In totaal waren de SGLT2-i nierbeschermend en verlaagden zij de samenstelling van verslechtering van nierfunctie, eindstadium nierziekte of renale sterfte met 45% (HR: 0.55, 95%CI: 0.48-0.64, P<0.0001), wat vergelijkbaar was tussen patiënten met ASCVD (HR: 0.56, 95%CI: 0.47-0.67, P<0.0001) en diegenen met meerdere risicofactoren (HR: 0.54, 95%CI: 0.42-0.71,P<0.0001) (P-interactie=0.71).
- De reductie in het samengestelde renale eindpunt werd gezien bij alle baseline eGFR-waarden, maar deze was het grootst in diegenen met behouden nierfunctie bij baseline, met een 33% reductie in de lage eGFR-groep (HR: 0.67, 95%CI: 0.51-0.89, P=0.0054), 44% in de middelste groep (HR: 0.56, 95%CI: 0.46-0.70, P<0.0001) en 56% in de hoogste groep (HR: 0.44, 95%CI: 0.32-0.59, P<0.0001) (P-trend=0.0258).
- De reductie in HHF was 40% in de laagste eGFR-groep (HR: 0.60, 95%CI: 0.47-0.77, P<0.0001), 31% in de middelste groep (HR: 0.69, 95%CI: 0.57-0.83, P<0.0001) en een niet-significante 12% reductie in de hoogste groep (HR: 0.88, 95%CI: 0.68-1.13, P=0.31) (P-trend=0.0073).
- Het effect van baseline eGFR op MACE was minder duidelijk en liet een niet-significante trend (P=0.23) zien richting een hoger behandelvoordeel in de laagste eGFR-categorie.
Veiligheidsuitkomsten
- In de trials werd significante heterogeniteit gezien voor amputaties (I²=79.1%) en fracturen (I²=78.2%), waarbij een hoger risico gezien werd in een enkele trial.
- Diabetische ketoacidose liet een consistent hoger risico zien in patiënten behandeld met SGLT2-i vergeleken met placebo (HR: 2.20, 95%CI: 1.25-3.87, P=0.0060), maar eventaantallen waren lager dan 1 per 1000 patiëntjaren.
Conclusie
Deze meta-analyse van de EMPA-REG OUTCOME, CANVAS Program en DECLARE-TIMI 58 trials liet alleen matige voordelen met SGLT2-i op atherosclerotische MACE zien in diegenen met ASCVD. Daarentegen werden robuuste reducties in HHF en progressie van nierziekte gezien ongeacht de atherosclerotische risicocategorie en voorgeschiedenis van HF bij baseline.
Referenties
1. Piepoli MF, Hoes AW, Agewall S, et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: the Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J 2016; 37: 2315–81.
2. American Diabetes Association. 8. Pharmacologic approaches to glycemic treatment: standards of medical care in diabetes—2018. Diabetes Care 2018; 41 (suppl 1): S73–85.
3. Wiviott SD, Raz I, Bonaca MP, et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. New Engl J Med (in press).
